Hoewel de oorzaken van de ziekte van Alzheimer een mysterie blijven, biedt genetisch onderzoek nu aanwijzingen over hoe de ziekte zich ontwikkelt. We weten dat zeldzame genetische mutaties vroege Alzheimer kunnen veroorzaken, maar zowel genetische factoren als omgevingsfactoren spelen een rol bij de meer algemene, late vorm van de ziekte. Door informatie te verzamelen over de genetische samenstelling van duizenden mensen, hebben wetenschappers in onze groep en anderen zich bijna geïdentificeerd 30-genvarianten die meer voorkomen bij de ziekte.
De functie van veel van deze 'risicogenen' in de hersenen is onbekend, maar ze lijken te clusteren op biologische functie, waardoor we meer inzicht krijgen in de mechanismen die betrokken zijn bij de ziekte van Alzheimer. Een van de biologische functies die betrokken zijn bij Alzheimer van deze genetische bevindingen is het transport van materiaal naar de cel, bekend als endocytose. Dit gebeurt wanneer het materiaal het celmembraan niet passief kan passeren, de cel naar binnen kuiert om de lading in een kleine met vloeistof gevulde zak te vangen.
Onze onderzoeksgroep onderzoekt wat deze endocytische genen in de hersenen doen. Met behulp van cellen die in een schaal zijn gegroeid, kunnen we de eiwitten die ze tot expressie brengen manipuleren en veranderingen in de opname van materiaal door de cel meten. Dit helpt ons te begrijpen wat er gebeurt als deze genen een verminderde werking hebben bij de ziekte van Alzheimer.
Endocytose is een universeel belangrijke celfunctie, alle cellen moeten eten en drinken. Het is ook verantwoordelijk voor vele andere vitale taken, waaronder communicatie, transport en opruimen van afvalproducten, zoals bèta-amyloïde. Dit is een eiwit dat wordt geproduceerd in het gezonde brein dat normaal wordt afgebroken en geëlimineerd. Bij de ziekte van Alzheimer wordt echter gedacht dat een verstoring van de bèta-amyloïde productie en de verwijdering ervan uit de hersenen veroorzaakt een opbouw en de vorming van kleverige klonten, bekend als plaques, die toxisch zijn voor neuronen.
Hersehuishouding
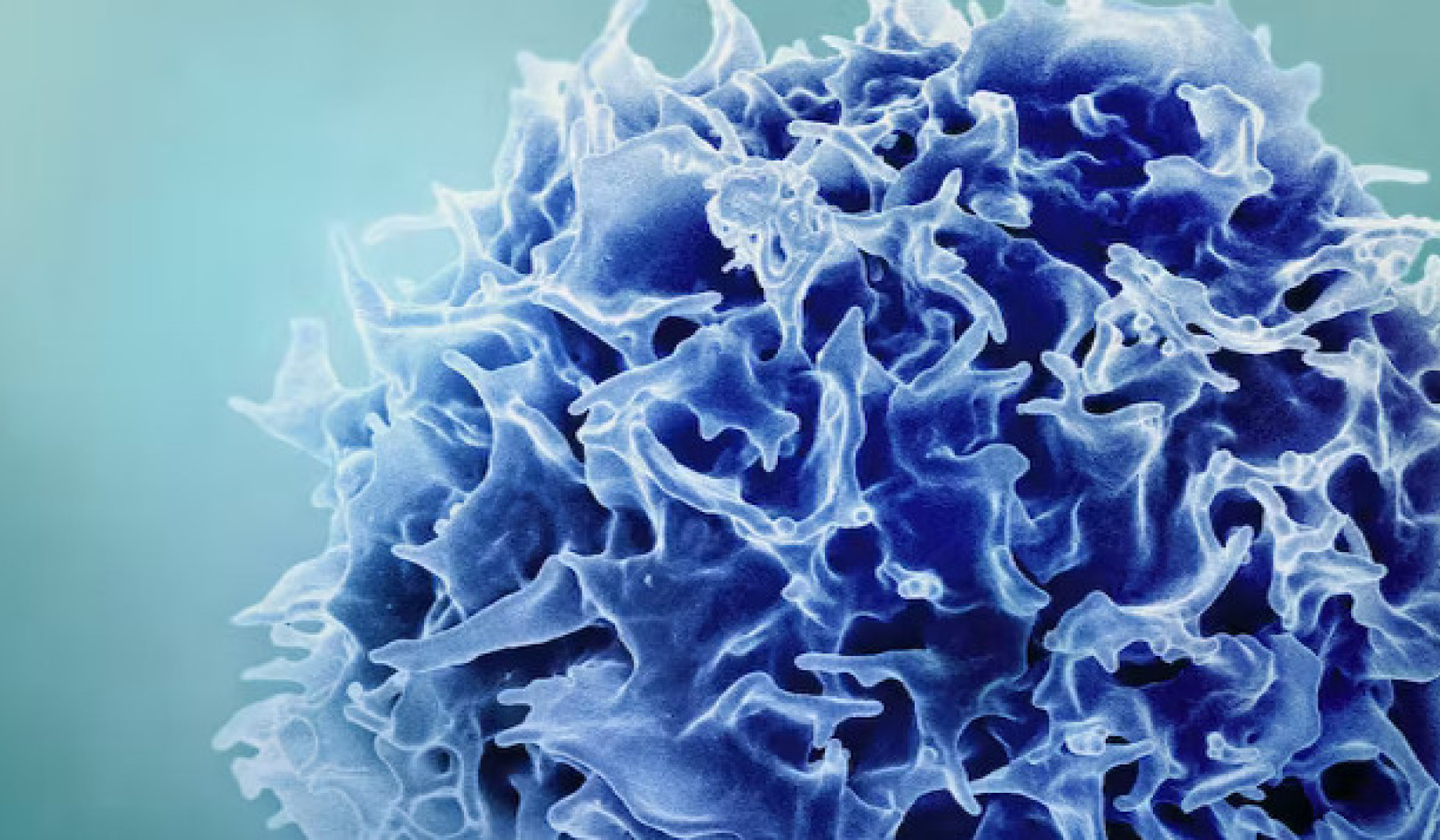
Het opruimen van beta-amyloïde is een van de functies die worden uitgevoerd door microglia, de immuuncellen van de hersenen. Zij zijn de eerste responders wanneer een indringer de hersenen binnenkomt. Ze gebruiken hun endocytische vermogens om afvalmateriaal en infectieuze stoffen te verzwelgen en te vernietigen. Bij Alzheimer is deze functie van cruciaal belang omdat ze bèta-amyloïde consumeren en het afbreken via hun interne afvalverwijderingssysteem.
Bèta-amyloïde kan ook via de 650km van bloedvaten in het hele menselijk brein worden verwijderd. De endotheelcellen die de bloedvaten vormen, vormen een nauwe barrière tussen het bloed en de hersenen. Dit stopt giftige stoffen, maar laat voedingsstoffen binnen en afvalproducten ontsnappen. Bèta-amyloïde wordt uit de hersenen verwijderd door een speciale vorm van endocytose waarbij het bindt aan een receptor op het oppervlak van endotheelcellen, zoals een slot en een sleutel. Dit triggert zijn internalisatie en wordt door de cel gedragen en in het bloed afgezet, het voorkomen van een opeenhoping in de hersenen.
Hoe komt beta-amyloïde er in de eerste plaats?
De precieze functie van beta-amyloïde is nog steeds onduidelijk, maar het is waarschijnlijk dat het een rol speelt in de normale hersenfysiologie, maar alleen een probleem wordt wanneer het in overmaat aanwezig is. Het wordt geproduceerd door de afbraak van het amyloïde precursor-eiwit (APP), gevonden op het oppervlak van cellen in de hersenen.
APP kan worden opgesplitst in twee verschillende manieren, waarvan er slechts één beta-amyloïde produceert. Het enzym dat verantwoordelijk is voor deze route bevindt zich in de cel, dus APP moet endocytose ondergaan om te worden verbroken tot beta-amyloïde fragmenten.
Een deel van ons onderzoek betreft het meten van de hoeveelheid bèta-amyloïde en andere fragmenten geproduceerd door cellen als gevolg van APP-afbraak. Door deze te vergelijken tussen gezonde cellen en cellen waarin de risico-genen van Alzheimer zijn gemanipuleerd, begrijpen we de betrokkenheid van deze genen bij de productie van beta-amyloïden. Ook hier lijkt endocytose een cruciale speler in de potentiële ontwikkeling van de ziekte van Alzheimer.
Dit illustreert slechts drie voorbeelden van hoe endocytose belangrijk is voor de gezondheid van de hersenen en hoe een fout in een van deze factoren een bijdragende factor kan zijn voor de ontwikkeling van Alzheimer. Inderdaad, vele andere biologische processen zijn in verband gebracht met genetische studies en het is onwaarschijnlijk dat ze elkaar uitsluiten. Met de toevoeging van zowel leefstijl- als omgevingsrisicofactoren is Alzheimer zeer complex. Niettemin kunnen we, door de verschillende betrokken mechanismen te begrijpen, mogelijke doelen voor behandeling gaan identificeren. Heel erg zoals een puzzel, gebruiken wij genetische informatie als hoekstukken om een duidelijker beeld van de ziekte als geheel op te bouwen.
Over de auteur
Anna Burt, PhD-onderzoeker, Cardiff University
Dit artikel is oorspronkelijk gepubliceerd op The Conversation. Lees de originele artikel.
Related Books:
at InnerSelf Market en Amazon